Czym jest tętniak mózgowy?
Tętniak mózgowy to miejscowe poszerzenie ściany naczynia krwionośnego w mózgu, przypominające niewielką „bańkę”. Największym zagrożeniem jest jego pęknięcie, które prowadzi do krwotoku podpajęczynówkowego – stanu bezpośrednio zagrażającego życiu.
Rokowanie po pęknięciu tętniaka [1–3]
- 10–15% pacjentów umiera przed dotarciem do szpitala
- Śmiertelność szpitalna wynosi 13–20%
- Śmiertelność roczna u leczonych pacjentów: około 23%
- Śmiertelność 5-letnia: około 29%
- 64% pacjentów żyje bez niepełnosprawności po 5 latach
- 36% ma zły wynik (śmierć lub niepełnosprawność) po 5 latach
Pomimo leczenia nawet pacjenci z dobrym wynikiem funkcjonalnym mogą doświadczać problemów poznawczych (np. z pamięcią lub koncentracją) (40–70%), depresji (33%), lęku (15–20%) oraz trudności z powrotem do pracy [2,4].
W celu zapobiegania pęknięciu tętniaka stosuje się dwie główne strategie leczenia:
- klipsowanie chirurgiczne (operacja otwarta)
- leczenie endowaskularne (przez naczynia krwionośne)
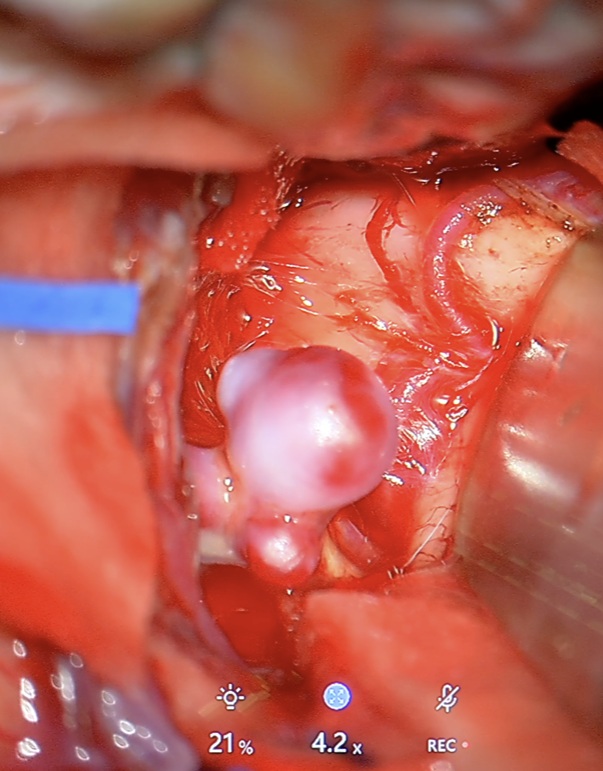
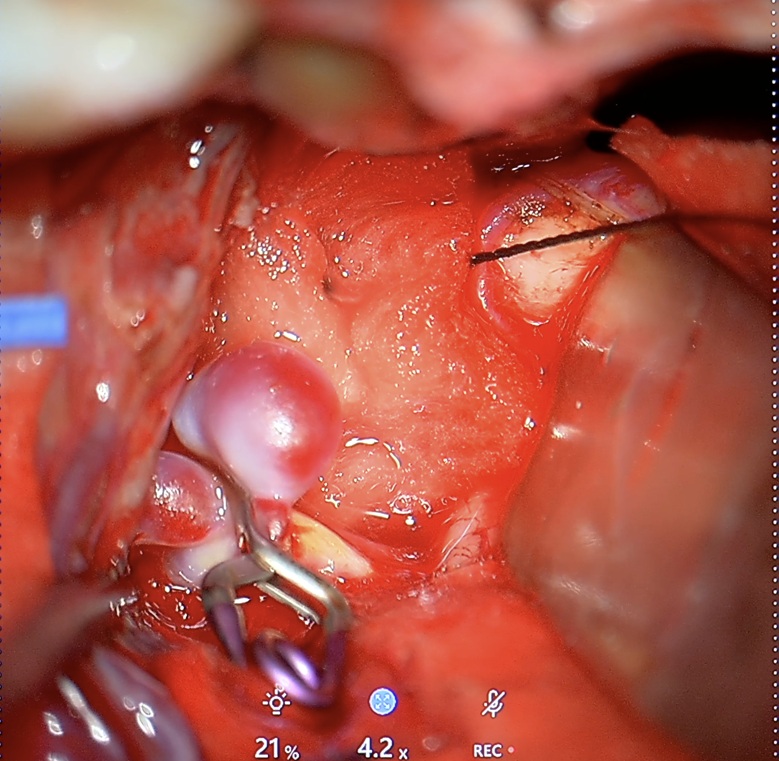
Klipsowanie chirurgiczne – metoda klasyczna
Jak przebiega zabieg?
Jest to operacja neurochirurgiczna, podczas której wykonuje się kraniotomię (czyli czasowe otwarcie fragmentu kości czaszki, aby uzyskać bezpieczny dostęp do mózgu). Pod mikroskopem operacyjnym neurochirurg zakłada tytanowy klips na szyję tętniaka, trwale odcinając dopływ krwi do jego wnętrza, przy jednoczesnym zachowaniu prawidłowego przepływu w naczyniu macierzystym (głównej tętnicy).
Cel leczenia
- trwałe i definitywne wyłączenie tętniaka z krążenia
- brak konieczności dalszych zabiegów i kontroli dożywotnich w większości przypadków
Kiedy klipsowanie jest najlepszym wyborem?
- tętniaki o szerokiej szyi
- tętniaki o złożonej budowie z odgałęzieniami
- lokalizacje takie jak MCA (tętnica środkowa mózgu), ICA (tętnica szyjna wewnętrzna), ACoA (tętnica łącząca przednia)
- młodsi pacjenci z długą oczekiwaną przeżywalnością
Leczenie endowaskularne (od środka tętnicy)
Jak przebiega zabieg?
Jest to procedura małoinwazyjna. Cewnik wprowadzany jest przez tętnicę udową (rzadziej promieniową) i prowadzony do naczyń mózgu. Następnie tętniak wypełnia się platynowymi spiralami (coiling). W wybranych przypadkach stosuje się dodatkowo balon, stent lub flow-diverter.
Nowoczesne techniki
- flow-divertery – przekierowują przepływ krwi poza tętniak
- specjalne urządzenia umieszczane bezpośrednio wewnątrz worka tętniaka (np. system WEB), które zaburzają przepływ krwi w jego wnętrzu [5]
Kiedy preferuje się leczenie endowaskularne?
- tętniaki tylnego krążenia mózgowego (np. szczyt tętnicy podstawnej, PICA)
- pacjenci w podeszłym wieku
- choroby współistniejące zwiększające ryzyko operacji otwartej
- pacjenci w ciężkim stanie klinicznym
Porównanie metod – w skrócie
Poniższa tabela pokazuje ogólne różnice między metodami leczenia. W konkretnym przypadku decyzja terapeutyczna zależy przede wszystkim od lokalizacji tętniaka, jego budowy oraz stanu ogólnego pacjenta.
| Cecha | Klipsowanie | Leczenie endowaskularne | Źródła |
| Inwazyjność | większa | mniejsza | [1] |
| Trwałość efektu | bardzo wysoka | umiarkowana | [2–4] |
| Ryzyko nawrotu | niskie (~5%) | wyższe (8–15%) | [2,4,5] |
| Ryzyko ponownego krwawienia (10 lat) | 0,03%/rok | 0,1%/rok | [6,7] |
| Kontrole obrazowe | zwykle niepotrzebne | konieczne | [2,3] |
| Pobyt w szpitalu | 6–8 dni | 3–5 dni | [1] |
| Rekonwalescencja | wolniejsza | szybsza | [1] |
| Powikłania (tętniaki niepęknięte) | 6,6–13,2% | 3,5–8,1% | [1] |
| Śmiertelność (tętniaki niepęknięte) | 0,6–2,5% | 0,6–0,9% | [1] |
Znaczenie lokalizacji tętniaka
Nie istnieje jedna najlepsza metoda leczenia dla wszystkich pacjentów. Kluczowe znaczenie mają:
- lokalizacja tętniaka
- jego kształt i wielkość
- wiek i stan ogólny pacjenta
- doświadczenie ośrodka neurochirurgicznego
Przykładowo:
- tętniaki MCA (tętnicy środkowej mózgu) i ACoA (tętnicy łączącej przedniej mózgu) częściej kwalifikują się do klipsowania ze względu na lepszą trwałość okluzji [13–16]
- tętniaki szczytu tętnicy podstawnej (BA) najczęściej leczone są endowaskularnie ze względu na głęboką lokalizację i trudny dostęp chirurgiczny [6,17]
- w tętniakach PICA (tętnicy tylnej dolnej móżdżku) obie metody są możliwe, przy czym klipsowanie daje trwalszą okluzję [6]
- tętniaki PCoA (tętnicy łączącej tylnej mózgu) z porażeniem nerwu okoruchowego mogą być leczone obiema metodami, choć klipsowanie prowadzi do szybszego ustąpienia objawów [18–21]
Szczegółowe porównanie metod w zależności od lokalizacji tętniaka
Różne lokalizacje tętniaków mogą wymagać różnych metod leczenia. Poniżej przedstawiono najczęstsze miejsca ich występowania oraz porównanie wyników leczenia dla każdej z nich.
Tętniaki ACoA (tętnica łącząca przednia)
| Cecha | Klipsowanie | Leczenie endowaskularne | Źródła |
| Całkowita okluzja tętniaka | 95–98% | 38–75% | [1–3] |
| Ryzyko ponownego leczenia | ~2% | 10–16% | [1,2] |
| Śmiertelność | podobna | podobna | [1] |
| Wynik funkcjonalny | podobny | podobny | [1] |
| Pobyt w szpitalu | 6–8 dni | 3–5 dni | [7,8] |
Interpretacja:
Ze względu na bardzo wysoką trwałość zamknięcia tętniaka klipsowanie często daje najtrwalszy efekt leczenia, szczególnie u młodszych pacjentów. Wyniki funkcjonalne są podobne w obu metodach [7,8,22].
Tętniaki MCA (tętnica środkowa mózgu)
| Cecha | Klipsowanie | Leczenie endowaskularne | Źródła |
| Całkowita okluzja (1 rok) | 71–89% | 31–54% | [1–3] |
| Ryzyko ponownego leczenia | ~3% | 8–15% | [1,2,4] |
| Powikłania | 7–10% | 5–7% | [2,13,15] |
| Wynik funkcjonalny | podobny | podobny | [1–3] |
| Pobyt w szpitalu | 6–9 dni | 3–5 dni | [6] |
Interpretacja:
Tętniaki MCA często mają szeroką szyję i odgałęzienia, dlatego klipsowanie pozwala na lepszą kontrolę anatomii i trwalszą okluzję. Klipsowanie pozostaje standardem leczenia w tej lokalizacji [13–16,23].
Tętniaki ICA (tętnica szyjna wewnętrzna)
| Cecha | Klipsowanie | Leczenie endowaskularne | Źródła |
| Trwałość okluzji | bardzo wysoka | umiarkowana | [6,12] |
| Powikłania (tętniaki niepęknięte) | 6–9% | 4–6% | [1] |
| Śmiertelność (tętniaki niepęknięte) | 0,6–2,5% | 0,6–0,9% | [1] |
| Pobyt w szpitalu | 5–7 dni | 3–4 dni | [1] |
Interpretacja:
W wielu przypadkach możliwe są obie metody, a wybór zależy od dokładnej lokalizacji tętniaka i jego relacji do ważnych gałęzi tętnicy [6].
Tętniaki PCoA (tętnica łącząca tylna)
| Cecha | Klipsowanie | Leczenie endowaskularne | Źródła |
| Ustąpienie porażenia nerwu (krótkoterminowe) | szybsze (1–6 miesięcy) | wolniejsze | [1–4] |
| Ustąpienie porażenia nerwu (≥18 miesięcy) | 86–97,5% | 64–95% | [1,3] |
| Czas do ustąpienia objawów | 87 dni | 133 dni | [2] |
| Pobyt w szpitalu | 6–8 dni | 3–5 dni | [5] |
Interpretacja:
Klipsowanie prowadzi do szybszego ustąpienia porażenia nerwu okoruchowego, ale w długoterminowej obserwacji (≥18 miesięcy) obie metody dają podobne wyniki. Wybór metody powinien uwzględniać pilność ustąpienia objawów i preferencje pacjenta [18–21].
Tętniaki PICA (tętnica móżdżkowa dolna tylna)
| Cecha | Klipsowanie | Leczenie endowaskularne | Źródła |
| Trwałość okluzji | bardzo wysoka (~95%) | dobra, lecz mniej trwała | [6] |
| Ryzyko ponownego leczenia | niskie | wyższe | [6] |
| Pobyt w szpitalu | 7–10 dni | 4–6 dni | [6] |
Interpretacja:
Klipsowanie daje bardzo trwały efekt leczenia, jednak wybór metody musi uwzględniać bliskość struktur pnia mózgu odpowiedzialnych za podstawowe funkcje życiowe oraz doświadczenie zespołu [6].
Tętniaki BA – szczyt tętnicy podstawnej
| Cecha | Klipsowanie | Leczenie endowaskularne | Źródła |
| Powikłania | wyższe | niższe | [1,2] |
| Trwałość okluzji | wysoka | umiarkowana | [1,3] |
| Wynik funkcjonalny | podobny | podobny | [1] |
| Pobyt w szpitalu | 7–10 dni | 3–5 dni | [2] |
Interpretacja:
Ze względu na głęboką lokalizację i sąsiedztwo pnia mózgu leczenie endowaskularne jest najczęściej metodą pierwszego wyboru, a chirurgia jest zarezerwowana dla wybranych przypadków [6,17].
Dlaczego u dwóch pacjentów z podobnym tętniakiem można zaproponować różne leczenie?
Na wybór metody leczenia wpływają:
- dokładna lokalizacja i kształt tętniaka
- wiek pacjenta i choroby towarzyszące
- ryzyko ponownego leczenia w przyszłości
- doświadczenie zespołu leczącego w danej technice
- preferencje pacjenta po przedstawieniu wszystkich opcji
Dlatego decyzja o leczeniu zawsze zapada indywidualnie po analizie korzyści i ryzyka każdej z metod przez zespół neurochirurgów i neuroradiologów interwencyjnych.
Bibliografia
- Kane SF, Butler E, Sindelar BD. Nontraumatic subarachnoid hemorrhage and ruptured intracranial aneurysm: recognition and evaluation. Am Fam Physician. 2023;108(4):386–395.
- Hoh BL, Ko NU, Amin-Hanjani S, et al. 2023 guideline for the management of patients with aneurysmal subarachnoid hemorrhage. Stroke. 2023;54(7):e314–e370.
- Roquer J, Cuadrado-Godia E, Guimaraens L, et al. Short- and long-term outcome of patients with aneurysmal subarachnoid hemorrhage. Neurology. 2020;95(13):e1819–e1829.
- Claassen J, Park S. Spontaneous subarachnoid haemorrhage. Lancet. 2022;400(10355):846–862.
- Celik E, Ozpeynirci Y, Liebig T, et al. Comparison of angiographic outcomes and complication rates of WEB embolization and coiling for treatment of unruptured basilar tip aneurysms. Sci Rep. 2022;12(1):10899.
- Thompson BG, Brown RD, Amin-Hanjani S, et al. Guidelines for the management of patients with unruptured intracranial aneurysms. Stroke. 2015;46(8):2368–2400.
- Sattari SA, Shahbandi A, Lee RP, et al. Surgery or endovascular treatment in patients with anterior communicating artery aneurysm: systematic review and meta-analysis. World Neurosurg. 2023;175:31–44.
- Kendirlioglu BC, Sulaimanov U, Erginoglu U, et al. Comparative outcomes of microsurgical and endovascular treatment for ruptured and unruptured anterior communicating artery aneurysms. Neurosurg Rev. 2026;49(1):123.
- Lindgren A, Vergouwen MD, van der Schaaf I, et al. Endovascular coiling versus neurosurgical clipping for aneurysmal subarachnoid haemorrhage. Cochrane Database Syst Rev. 2018;8:CD003085.
- Rabelo NN, Telles JPM, Pipek LZ, et al. Long-term outcomes of ruptured saccular intracranial aneurysm clipping versus coiling. Neurol Sci. 2022;43(8):4909–4915.
- Eskey CJ, Meyers PM, Nguyen TN, et al. Indications for intracranial endovascular neurointerventional procedures. Circulation. 2018;137(21):e661–e689.
- Molyneux AJ, Birks J, Clarke A, Sneade M, Kerr RS. Durability of endovascular coiling vs clipping of ruptured cerebral aneurysms: ISAT 18-year follow-up. Lancet. 2015;385(9969):691–697.
- Zhang Z, Liu JY, Xing HS, Ma JY, Li AJ. Microsurgical clipping and endovascular intervention for middle cerebral artery aneurysm: meta-analysis. Medicine (Baltimore). 2023;102(34):e34956.
- Berro DH, L’Allinec V, Pasco-Papon A, et al. Clip-first policy versus coil-first policy for MCA aneurysms. J Neurosurg. 2020;133(4):1124–1131.
- Sturiale CL, Scerrati A, Ricciardi L, et al. Clipping versus coiling for treatment of MCA aneurysms: Italian multicenter experience. Neurosurg Rev. 2022;45(5):3179–3191.
- Darsaut TE, Keough MB, Sagga A, et al. Surgical or endovascular management of MCA aneurysms: randomized comparison. World Neurosurg. 2021;149:e521–e534.
- Winkler EA, Lee A, Yue JK, et al. Endovascular embolization versus surgical clipping of basilar artery aneurysms. Acta Neurochir (Wien). 2021;163(5):1527–1540.
- Abo Kasem R, Cunningham C, Elawady SS, et al. Oculomotor nerve palsy recovery following microsurgery vs endovascular treatment of PCoA aneurysms. Neurosurg Rev. 2024;47(1):904.
- Liu J, Peng C, Zhu G, et al. Surgical clipping vs endovascular coiling for PCoA aneurysm-induced oculomotor nerve palsy. Medicine (Baltimore). 2020;99(47):e22969.
- Shen X, Wang W, Qin H, Ren CF, Gao BL. Long-term results of endovascular vs surgical treatment of PCoA aneurysms with oculomotor nerve palsy. Medicine (Baltimore). 2022;101(34):e30421.
- Tian LQ, Fu QX. Recovery of PCoA aneurysm-induced oculomotor nerve palsy after clipping vs embolization. BMC Neurol. 2020;20(1):351.
- Haeren R, Hafez A, Korja M, Raj R, Niemelä M. Fast transition from open surgery to endovascular treatment of unruptured ACoA aneurysms. World Neurosurg. 2022;165:e668–e679.
- Pflaeging M, Kabbasch C, Schlamann M, et al. Microsurgical clipping versus advanced endovascular treatment of unruptured MCA bifurcation aneurysms. World Neurosurg. 2021;149:e336–e344.